Negli anni recenti sono stati registrati importanti sviluppi relativi alla disponibilità di farmaci altamente innovativi per la cura dell’emofilia, nonostante uno scenario precedente soddisfacente.
Per i pazienti con la forma grave del difetto, l’infusione endovena dei concentrati della coagulazione in regime di profilassi rappresenta il trattamento di scelta. La profilassi ha dimostrato di ridurre significativamente l’artropatia, limitare la frequenza dei sanguinamenti e migliorare la qualità della vita dei pazienti, dei loro famigliari o di altri ‘caregiver’. La profilassi con concentrati ricombinanti di fattore VIII (rFVIII) oppure di fattore IX (rFIX) tradizionali richiede l’infusione endovenosa regolare almeno due (rFIX) o tre (rFVIII) volte alla settimana. Oggi prodotti di rFVIII e di rFIX a ‘lunga azione’, anche definiti ad emivita prolungata, sono stati approvati in Italia e in altri Paesi, mentre altri sono ancora in fase di sviluppo. I preparati di rFVIII e di rFIX a ‘lunga azione’ hanno un’emivita 1,5-1,8 e 3-5 volte rispettivamente paragonata a quella dei prodotti standard. Questi nuovi prodotti posseggono il potenziale per affrontare molte delle esigenze non soddisfatte dei pazienti attualmente trattati con i concentrati tradizionali. Nella tabella seguente sono riportati i prodotti a ‘lunga azione’ approvati e quelli ancora in studio.
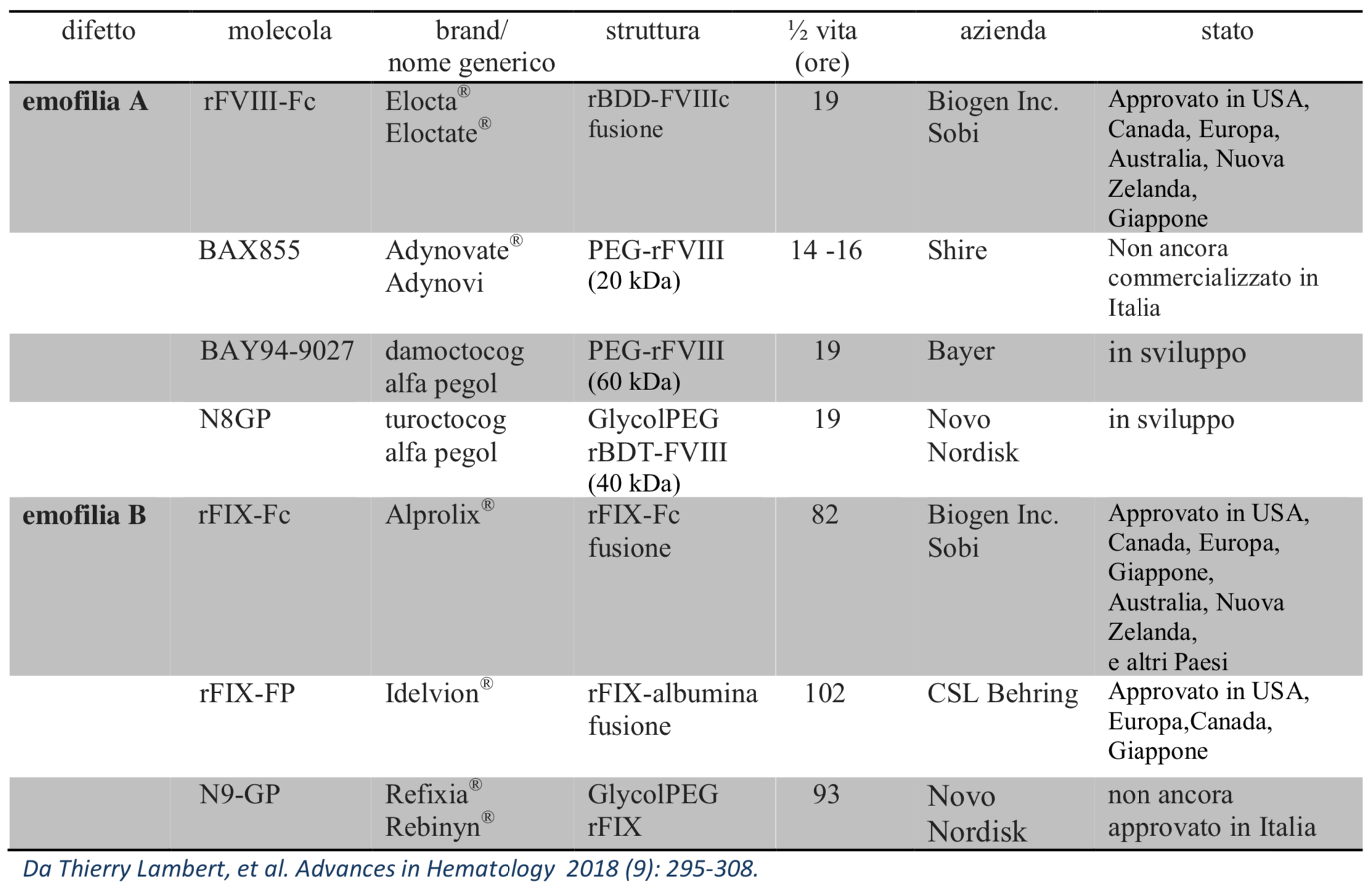
Le indicazioni rivenienti dagli studi clinici e riportate sulle rispettive schede tecniche dei preparati a ‘lunga azione’ sono la profilassi e il trattamento dell’emofilia. Attualmente, al contrario dei regimi standard, non vi è consenso circa la dose e gli intervalli ottimali tra le infusioni nella profilassi con questi prodotti.
Per quanto attiene all’emofilia A è dimostrato che il tempo trascorso con un ‘trough level‘ di FVIII inferiore all’1% è proporzionale all’incidenza dei sanguinamenti mentre un ‘trough level‘ superiore all’1% garantisce maggiore protezione contro le emorragie in particolare quelle articolari.Nella pratica clinica i concentrati ad azione prolungata consentono la riduzione della frequenza delle infusioni incoraggiano i pazienti a passare dal trattamento ‘a domanda’ alla profilassi riducono l’uso di cateteri venosi centrali nei bambini e infine tendono a migliorare la qualità della vita. In aggiunta a quanto descritto è fondamentale rimarcare che i preparati a ‘lunga azione’ aumentano il ‘trough level’ alla stessa dose utilizzata per i preparati standard prevengono emorragie spontanee e subcliniche contribuiscono a mantenere stabili le funzioni articolari. Per I pazienti con emofilia A la dose iniziale comunemente raccomandata per gli adulti si basa sul peso corporeo per 2 volte oppure ogni 3 – 4 giorni nella settimana (vs ogni 2 giorni con il rFVIII standard).
Nei bambini l’emivita della maggior parte dei prodotti è più corta per cui anche gli intervalli tra le infusioni potranno essere più corti. La dose e i tempi di infusione potranno essere modificati in base al fenotipo emorrarragico e alla farmacocinetica (PK) individuali. Tuttavia nella pratica clinica gli studi di PK sono spesso poco eseguibili specie per i bambini a causa dei prelievi di sangue ripetuti. A questo problema si può in qualche modo ovviare con l’applicazione dei test farmacocinetici di ‘popolazione’ che adotterebbero meno prelievi con minori costi. I modelli di PK ‘di popolazione’ consentono di studiare le sorgenti della variabilità nella popolazione nonché le variabili correlate a tale variabilità di quantificare le componenti inspiegate e di trattare i dati come un unico individuo.
Negli adulti con emofilia B il regime di profilassi con concentrati ad emivita prolungata prevede la dose inziale di una volta la settimana vs quella di due volte la settimana con i prodotti standard. Epperò in alcuni pazienti ben controllati è possibile estendere l’intervallo della dose ogni 10-14 giorni. Anche per i bambini con emofilia B alcuni prodotti hanno dimostrato di avere un’emivita più corta per cui è ragionevole mantenere la dose iniziale a una volta la settimana. E’ oggetto di dibattito se il ‘trough level’ efficace con i preparati di rFIX debba essere superiore (10-20 U.I./dl) a quello di mantenimento per l’rFVIII.
Per quanto attiene gli studi di PK nei pazienti che utilizzano prodotti di rFIX ad emivita prolungata valgono le stesse considerazioni descritte per i prodotti di rFVIII. Anche in questo caso gli studi di PK ‘di popolazione’ sembrerebbero più applicabili nella pratica clinica.In corso di profilassi con i prodotti ad azione prolungata risulta utile eseguire il dosaggio dei FVIII/FIX E’ noto che il controllo di laboratorio può essere eseguito con un test coagulativo ‘one stage’ oppure con metodica cromogenica. Vi sono evidenze che i due test registrano discrepanze nei risultati sovrastimando o sottostimando la concentrazione ematica dei fattori di preparati sia standard che ad azione prolungata. L’utilizzo di un test piuttosto che un altro è affidato alla competenza dello specialista e del laboratorio.
Un sondaggio sullo switch ai preparati ad emivita prolungata e la percezione dello sviluppo di inibitore mostra tale perplessità nel 57% dei pazienti e nel 20% dei medici. Studi clinici non dimostrano un aumento del rischio di inibitori nello switch da un plasma derivato ad un prodotto ricombinante oppure da un rFVIII ad un altro (inclusi i ‘full lenght’ e i B-domain-deleted/trunked). Gli studi clinici condotti sui PTPs con switch da preparati standard a prodotti ad emivita prolungata hanno dimostrato l’assenza o il bassissimo rischio di sviluppo di inibitore. Nella pratica clinica non si ravvisa nessuna controindicazione per lo switch negli emofilici adulti. In attesa dei risultati di studi clinici condotti sui pazienti pediatrici che non abbiano ancora iniziato il trattamento sostitutivo (Previous Untreated Patients: PUPs) è ragionevole effettuare lo switch ai preparati ad emivita prolungata dopo che il bambino abbia superato le 50 esposizioni con il prodotto standard.
Lo switch ai preparati ad emivita prolungata è particolarmente raccomandata nei pazienti specie se adolescenti con scarsa aderenza alla profilassi tradizionale in quelli con attivitàlavorativa/sportiva particolarmente a rischio di traumi e negli emofilici con fenotipo emorragico grave.Non vi sono evidenze scientifiche che controindichino l’uso di preparati ad emivita prolungata negli emofilici che abbiano eradicato l’inibitore con l’immunotolleranza purchè trascorra un tempo sufficientemente lungo per scagionare la recidiva (~ 6-12 mesi). E’ da annotare che il riscontro in alcuni emofilici di un livello più alto di fattore von Willebrand endogeno influenza positivamente il livello di fattore VIII dei prodotti standard e di quelli a ‘lunga azione’.
A conclusione di quanto espresso sull’adozione nella pratica clinica dei concentrati anti-emofilici ad emivita prolungata si raccomanda di monitorare e aggiustare la dose del prodotto e la frequenza delle infusioni fino a raggiungere un ‘trough level’ di mantenimento efficace di informare correttamente il paziente per non deludere le aspettative particolarmente per chi utilizzerà preparati con FVIII.Inoltre in pazienti con fenotipo emorragico grave il regime di profilassi con i preparati di rFVIIII a ‘lunga azione’ può essere simile a quello utilizzato con i preparati standard. Infine i pazienti che sanguinano acutamente durante la profilassi con questi preparati devono utilizzare lo stesso prodotto a dose congrua e comunque ridotta rispetto a quella utilizzata nel trattamento con i concentrati tradizionali..Sebbene l’introduzione nella pratica clinica dei prodotti a ‘lunga azione’ rimane da valutare sotto alcuni punti di vista (compresi i costi, la sicurezza e il follow-up a lungo termine dei pazienti) i nuovi preparati attualmente disponibili e in fase di sviluppo rappresentano un potenziale straordinario che comporta cambiamenti significativi nel trattamento dell’emofilia.
Letture suggerite
– Thierry Lambert, Gary Benson, Gerry Dolan, et al. Advances in Hematology 2018 (9): 295-308.
– Mancuso ME and Santagostino E. Outcome of Clinical Trials with New Extended Half-Life FVIII/IX Concentrates. J Clin Med 2017; 6: E39.
– Ljung R, Fischer K, Carcao M, et al. Practical considerations in choosing a factor VIII prophylaxis regimen: role of clinical phenotype and trough levels. Thromb Haemost 2016; 115: 913–920.
– Morfini M. The history of clotting factor concentrates pharmacokinetics. J Clin Med 2017; 6: E35.