La conferma nei risultati finali dello studio di estensione del Protect VIII
Recentemente su Haemophilia ( DOI: 10.1111/hae.14297) sono stati pubblicati i dati finali dello studio di estensione del Protect VIII. Il BAY 94–9027(damoctocog alfa pegol; Jivi®) è un ricombinante del F.VIII (rFVIII) sito-specifico coniugato con polietilenglicole (PEG) on l’obbiettivo di ridurre la clearance e di prolungare la sua permanenza in circolo.
I risultati del PROTECT VIII hanno dimostrato una eccellente efficacia e un’assoluta sicurezza del damoctocog (BAY 94–9027) nella prevenzione e nel trattamento degli episodi emorragici sia negli adulti che negli adolescenti con emofilia grave A. Al termine dello studio si è data la possibilità ai pazienti di continuare con il trattamento e di valutare, in un lungo arco temporale, la sicurezza e l’efficacia dopo 100 giorni di esposizione al farmaco.
Lo studio sopra citato riporta i dati finali con un follow up fino a sette anni. Questo lavoro osservazionale ha raccolto i pazienti che nello studio primario avevano completato le 36 settimane di osservazione. Le caratteristiche dello studio è stato di essere aperto, facoltativo, non controllato e condotto in 53 centri di 18 nazioni differenti (nella tab.1 sono riportati i vari regimi terapeutici scelti dai pazienti).
121 pazienti, tra i 12 e i 65 anni, dei 134 arruolati nel PROTECT VIII hanno partecipato allo studio di estensione e rappresentato l’oggetto dell’analisi di questo lavoro. Nella tab.1 sono riportate le caratteristiche della malattia e i dati demografici dei pazienti mentre nella fig. 1 vengono mostrati i regimi terapeutici dal termine dello studio principale a quello di estensione.
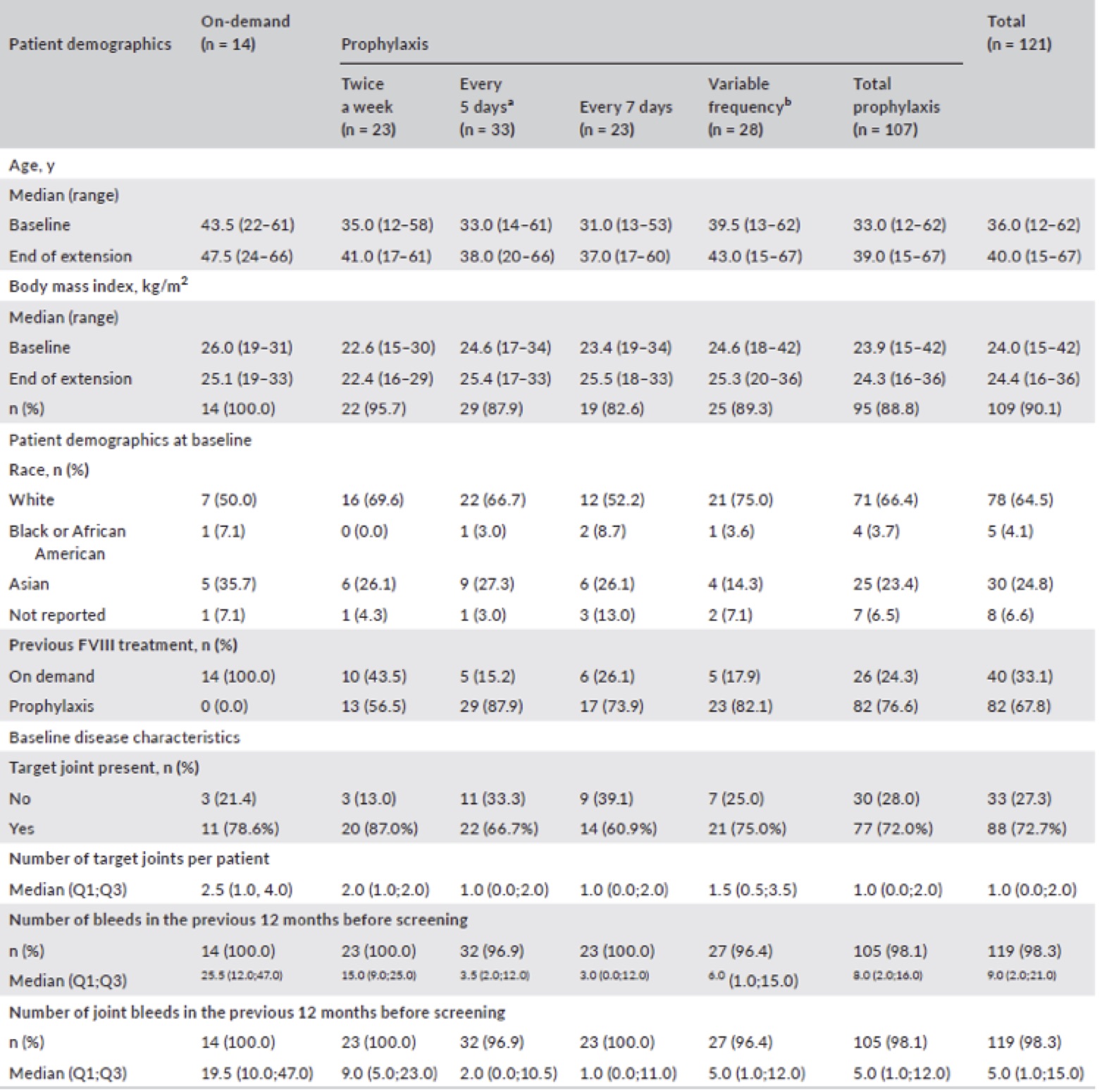
Tab.2 – Caratteristiche e dati demografici dei pazienti all’ingresso e al termine dello studio
In definitiva 83 soggetti su 107 ha mantenuto lo stesso programma terapeutico che avevano al termine dello studio primario. Un secondo gruppo chiamato VAR (soggetti che hanno variato il regime terapeutico nel corso dello studio di estensione) ha raccolto 28 pazienti così divisi: 20 sono passati da un programma terapeutico con una frequenza di trattamento più bassa ad una più alta, 4 pazienti al contrario da una più bassa ad una più alta frequenza e 4 che hanno cambiato frequenza più volte.
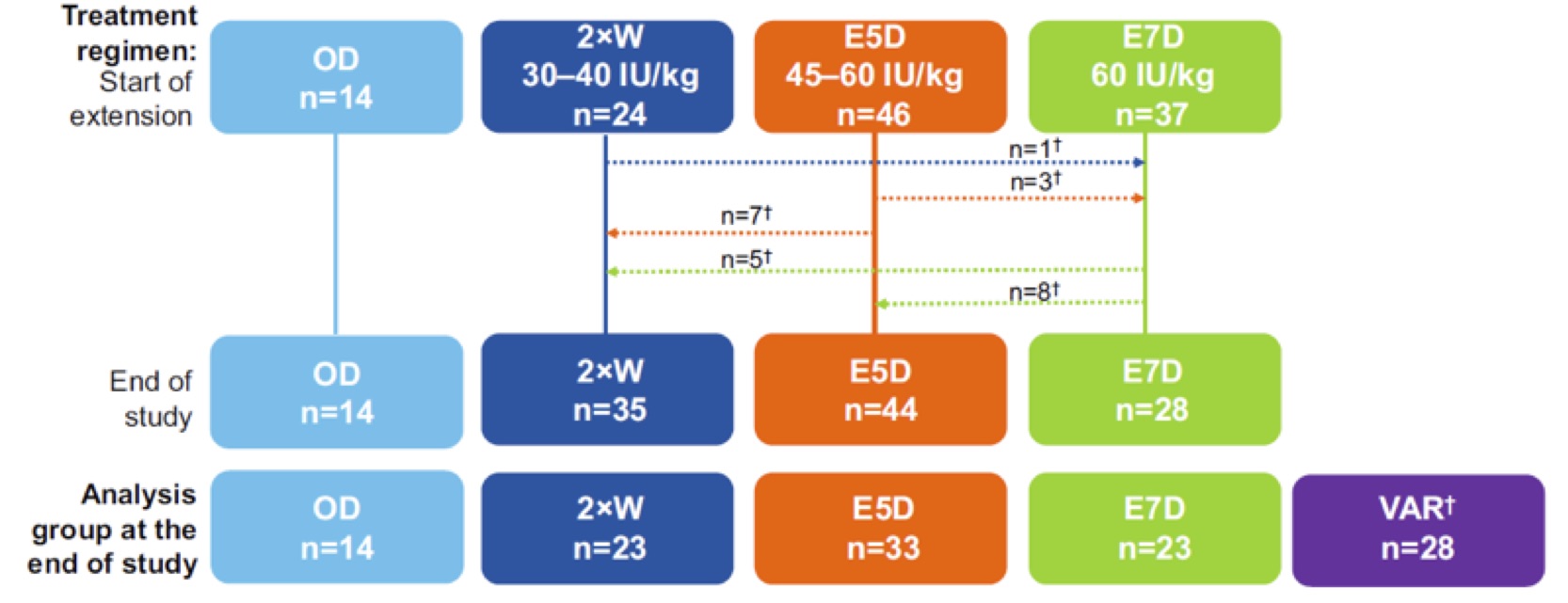
Fig. 1 – Collocamento dei pazienti nei vari gruppi di trattamento dall’inizio alla fine dello studio di estensione. I pazienti che hanno cambiato regime terapeutico nella prima settimana dello studio di estensione sono stati inseriti nel gruppo VAR. 2xW ( 2volte settimana) E5D ( ogni 5 giorni ) E7D ( ogni 7 giorni) OD ( a domanda).
In sintesi possiamo riassumere come segue i risultati. L’ABR totale mediano, ovvero il tasso di sanguinamento annuale, (Q1; Q3) durante lo studio di estensione è stato di 1,49 (0,36; 4,80) per tutti i pazienti in profilassi (n = 107), rispetto a 34.09 (20.3; 36.6) per i pazienti on-demand (n = 14).
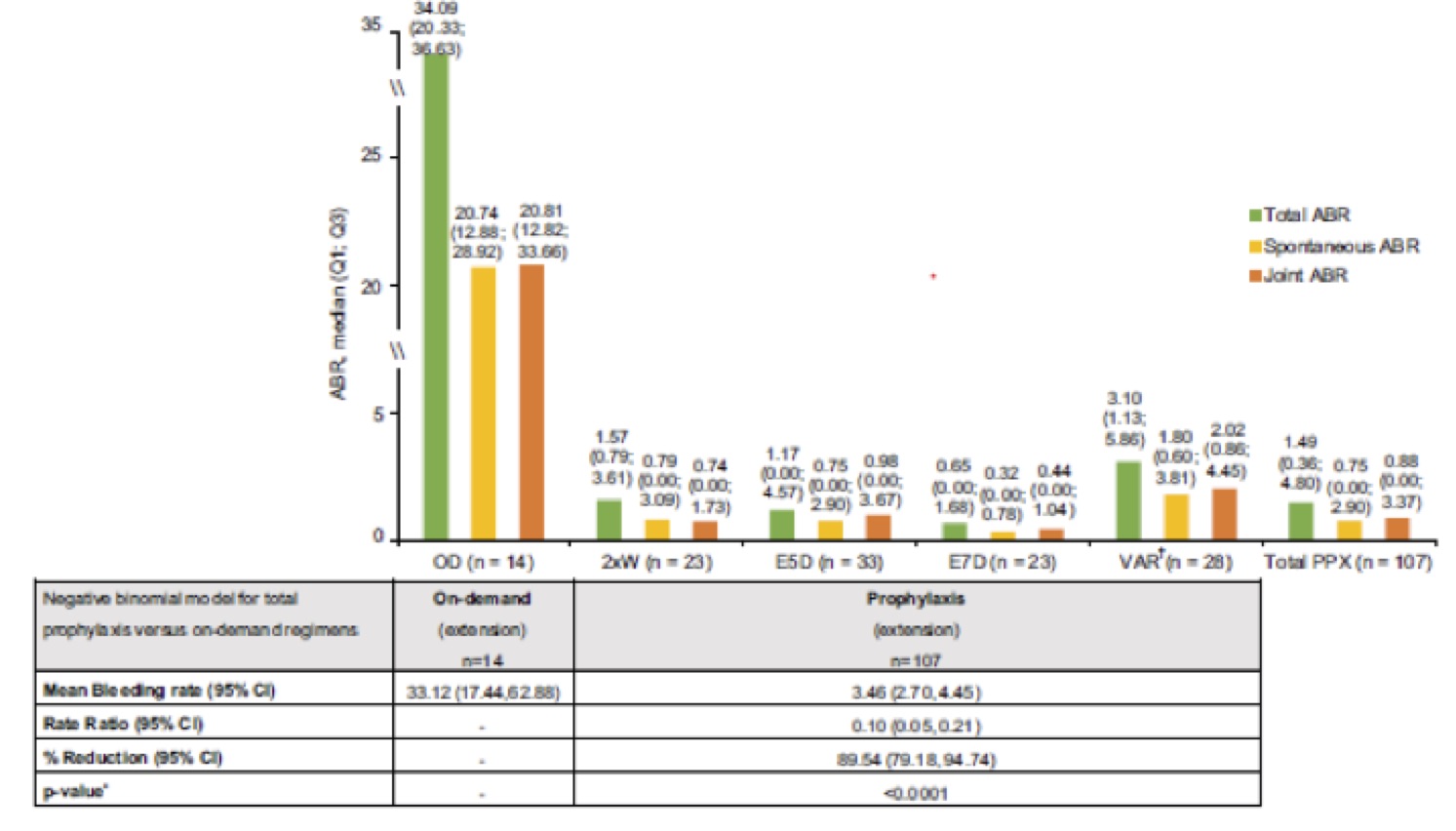
Figura 2 – ABR nello studio di estensione Protect VIII. PPX profilassi, OD a domanda, Q quartile
In particolare tra i pazienti in profilassi che non hanno mai modificato regime posologico, l’ABR totale mediano era <2,0 (Figura 2).
Comunque sia i sanguinamenti spontanei sono stati osservati ridursi in tutti i regimi di profilassi se paragonati al gruppo in trattamento a domanda: rispettivamente 0.75 (0,0; 2,9) vs 20,74 (12,9; 28,9) (Figura 2).
L’ABR articolare per i pazienti con profilassi era 0,88 (0,0; 3,37), rispetto a un ABR articolare mediano di 20,81 (12,3; 33,7) per i pazienti trattati su richiesta.
Infine nel corso della partecipazione allo studio di estensione, il 20,6% dei pazienti sottoposti a profilassi non ha presentato nessun tipo di sanguinamento e il 29,9% non ha presentato sanguinamenti articolari (Figura 3).
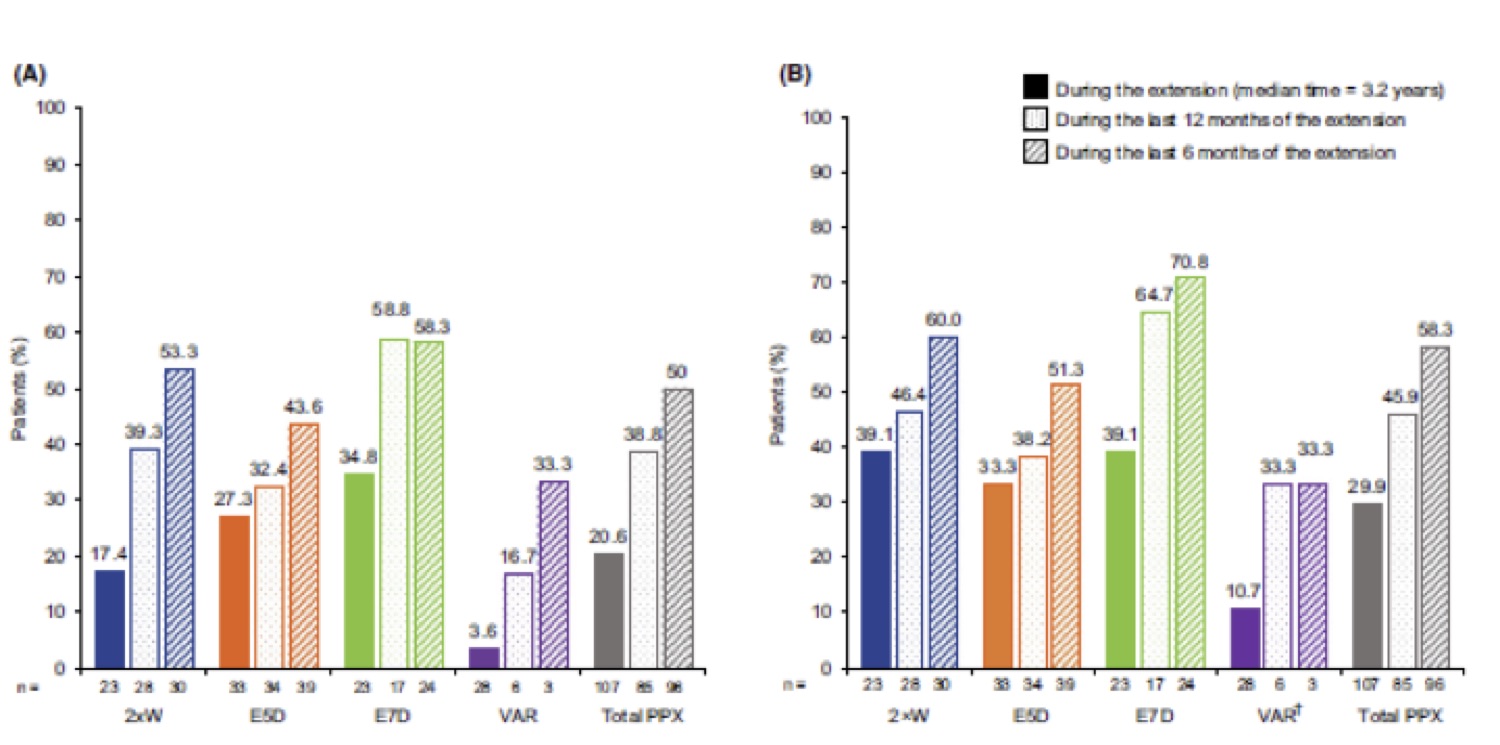
Figura 3 Pazienti con nessun sanguinamento totale (A) o articolare (B) nello studio.
Se poi si si osservano i dati dei pazienti (n = 85) che correttamente hanno partecipato agli ultimi 12 mesi dello studio si rileva come il 38,8% non abbia presentato nessun tipo di sanguinamento ed il 45,9 % non avesse presentato sanguinamenti articolari. Se infine l’osservazione viene fatta negli ultimi sei mesi di partecipazione allo studio, i pazienti non hanno presentato rispettivamente sanguinamenti totali per il 50,0 % e articolari per il 58,3%.
Gli autori concludono che il Bay 94–9027 è stato ben tollerato durante tutto il periodo di estensione del PROTECT VIII: nessun paziente ha sviluppato inibitori del FVIII e la maggior parte dei pazienti non ha avuto livelli di PEG rilevabile nel plasma.
Questo è stato osservato solo in alcuni pazienti in modo saltuario e transitorio.
I marcatori della funzionalità renale ed epatica nei sette anni di osservazione sono sempre stati entro i limiti normali Questi dati supportano dunque il favorevole rapporto rischio-beneficio profilo di BAY 94–9027 e il suo utilizzo a lungo termine per i pazienti con emofilia A.
Lo studio di estensione PROTECT VIII riporta il più lungo follow-up di qualsiasi altro studio di estensione su adolescenti e adulti con emofilia grave A.
L’ABR si è confermato basso in tutte le condizioni in cui era praticata la profilassi e questo risultato è stato mantenuto per ≥5 anni utilizzando programmi di infusione adattati alle esigenze dei singoli pazienti e con un basso consumo annuale di FVIII.
Il BAY 94-9027 dunque secondo gli autori è in grado di assicurare una eccellente gestione dell’emofilia A permettendo ai pazienti di assicurare la migliore qualità di vita attualmente possibile.
Per approfondire
- Coyle TE, Reding MT, Lin JC, Michaels LA, Shah A, Powell J. Phase I study of BAY 94–9027, a PEGylated B-domain-deleted recombinant factor VIII with an extended half-life, in subjects with hemophilia A. J Thromb Haemost. 2014;12(4):488-496.
- European Medicines Agency. Jivi (damoctocog alfa pegol) summary of positive opinion. 2018; https://www.ema.europa.eu/en/docum ents/smop-initi al/chmp-summary-positive-opinion-jivi_en.pdf. Reding MT, Ng HJ, Poulsen LH, et al. Safety and efficacy of BAY94–9027, a prolonged-half-life factor VIII. J Thromb Haemost. 2017;15(3):411-419.
- Lalezari S, Reding MT, Pabinger I, et al. BAY 94–9027 prophylaxis is efficacious and well tolerated for up to >5 years with extended dosing intervals: PROTECT VIII extension interim results. Haemophilia. 2019;25(6):1011-1019.



