Il Dolore nell’Emofilia un pianeta ancora sconosciuto: a Glasgow, nel corso del congresso WHF 2018, una sessione è stata dedicata a questo problema troppo spesso trascurato. Ne riportiamo qui una sintesi.
Il dolore nei pazienti con emofilia è stato ed è un problema tanto importante quanto negletto. La letteratura medica a questo riguardo, a differenza di altre condizioni cliniche, è priva di studi sui meccanismi fisiopatologici del dolore. L’approccio terapeutico a tale problema è sempre stato empirico e con risultati molto modesti.
Per andare all’entità del fenomeno, i sondaggi indicano che l’85% della popolazione emofilica adulta ha sofferto di dolore durante gli ultimi 6 mesi (1) e l’89% dei pazienti ha riferito che quel dolore aveva interferito con la loro vita quotidiana nelle ultime 4 settimane (2).
Inoltre, in pazienti con emofilia grave meno del 15% dichiara di provare dolore solo in 1 o 2 regioni, mentre oltre il 35% segnala sintomatologia dolorosa in almeno 5 regioni (3).
Comprendere invece i meccanismi del dolore predominante (dolore nocicettivo, neuropatico, alterazione del dolore centrale e influenze delle componenti psicologiche) è di estrema importanza giacche’ andrà ad indirizzare l’approccio terapeutico. Tradizionalmente, è sempre stata fatta una differenziazione tra il dolore derivante da un’emorragia acuta (emartrosi) e dolore cronico originato da danno articolare (artropatia) (4).
Questa definizione in realtà si dimostra assolutamente inadeguata a definire e caratterizzare il dolore emofilico. In primo luogo, i termini “acuto” e “cronico” originariamente si riferivano a un periodo di tempo e non a un causa sottostante specifica del dolore (5,6). In secondo luogo, sia i pazienti che i medici sembrano non essere in grado di differenziare i sintomi di emartrosi da quelli di artropatia, visto la grande sovrapposizione in sintomi clinici tra le due condizioni.(1,4,7,8).
Uno studio comparativo, condotto con ultrasuoni, sulle percezioni riguardanti l’eziologia del dolore ha confermato che una diagnosi basata sulla sola percezione del dolore è inaffidabile nella maggior parte dei casi: l’eziologia del dolore (sanguinamento contro infiammazione articolare o altra sindrome da dolore regionale) è stato giudicato correttamente solo nel 30% dei casi, dal medico e nell’8% dal paziente! (8)
Spesso ci si limitata alla valutazione soggettiva dell’intensità del dolore e ci si aiuta con l’uso di non convalidati questionari sul dolore (9). Non sorprende che un sondaggio tra 22 centri in Europa ha rivelato una incapacità di valutare in modo standardizzato il dolore e un alto livello di variabilità nella gestione dello stesso (10).
VERSO UNA MIGLIORE COMPRENSIONE DEL DOLORE
L’associazione internazionale per lo studio del dolore(International Association for the Study of Pain 1986) definisce il dolore come una spiacevole esperienza sensoriale ed emotiva associata a danno tissutale in atto o potenziale, o descritto in termini di danno.
Questa definizione implica che il danno tissutale potrebbe essere presente, e nello stesso tempo afferma che non è sempre necessario avere danni ai tessuti per provare dolore.
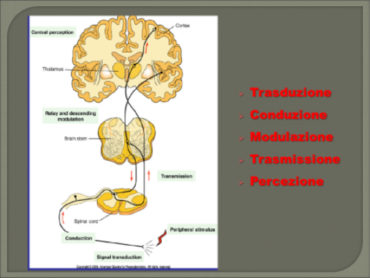
Il segnale doloroso, una volta generato, viene modulato (limitato o amplificato) a vari livelli (segmentario e centrale) da stimoli provenienti da strutture nervose (sensoriali, psichiche, della memoria…) e non (metaboliche, immunologiche), prima di arrivare, alle sedi naturali che ne danno l’interpretazione clinica. Si spiega così come il dolore sia il risultato di un complesso sistema di interazioni, dove diversi fattori (ambientali, culturali, religiosi, affettivi fisici) ne modulano, entità e caratteristiche.Il dolore dunque può essere esperienza individuale e soggettiva, a cui convergono componenti puramente sensoriali (nocicezione) relative al trasferimento dello stimolo doloroso dalla periferia alle strutture centrali, e componenti esperenziali e affettive, che modulano in maniera importante quanto percepito”.
Alcuni autori hanno condotto uno studio sullarelazione tra intensità del dolore (VAS) e danno articolare (11). Mentre confermano una correlazione tra intensità del dolore e la valutazione congiunta radiologica / clinica del danno per entrambe le ginocchia (punteggi di correlazione di Spearman >50), al contrario questa correlazione non era dimostrabile nel caso dei gomiti e delle caviglie (11) . Ciò conferma che può esistere una discordanza tra il dolore sperimentato dal paziente e la presunta causa periferica del dolore (12).
Quando una parte del nostro corpo si confronta con uno stimolo nocivo (che danneggia o minaccia di danneggiare), sia esso meccanico, chimico o termico le vie ascendenti di trasmissione trasmettono questa informazione dalla periferia al cervello. Le fibre nocicettive (A –deltamielinizzatee a conduzione rapidae C non mielinizzate a conduzione lenta) condurranno il segnale nocicettivo al corno dorsale del midollo spinale, la prima stazione centrale di ritrasmissione per l’elaborazione di stimoli nocicettivi (6,14).
Nel corno dorsale altri neuroni che potremmo chiamare di proiezione trasmetteranno ulteriormente le informazioni al talamo, attraverso la via spinotalamica controlaterale alla corteccia somatosensoriale primaria.
Il talamo cosìserve come secondo relè sinaptico, dove i suoi neuroni stabiliscono un legame sinaptico con i neuroni terziari.(14) .
Inoltre dobbiamo tener presente che connessioni dirette si stabiliscono sempre tra il corno dorsale e il midollo allungato, il tronco cerebrale e l’ipotalamo tramite le vie spinoreticulare, spinomesencephalica e spinoipotalamica (14,17).
Le regioni cerebrali corticali e sottocorticali, come la corteccia cingolata anteriore, l’insula, la corteccia prefrontale, la corteccia somatosensoriale e l’amigdala, spesso indicati come la matrice del dolore, sono attivati durante i processi nocicettivi e contribuiscono a diversi aspetti della percezione del dolore, inclusa la qualità sensoriale del dolore, la paura del dolore, la memoria del dolore e la modulazione del dolore (14,17,19).
E’ importante qui rimarcare che il dolore si verifica solo quando l’informazione raggiunge il cervello. Dobbiamo inoltre ricordare che il termine nocicezione viene usato per riferirsi agli impulsi nervosi che seguano la stimolazione nociva, mentre la percezione del dolore è un complesso sensoriale, affettivo e socioculturale; fenomeno che richiede attività del sistema nervoso centrale e del cervello (14,20). Il dolore è un fenomeno dinamico e i segnali nocicettivi saranno modulati a diversi livelli del sistema nervoso centrale (14). Questi sistemi di modulazione degli impulsi nel sistema nervoso periferico e centrale possono aumentare o diminuire la sensazione di dolore (20). Soprattutto i percorsi discendenti che trasportano segnali dal cervello alla dorsale il corno sono di grande importanza nella modulazione del dolore.

L’attività nei percorsi discendenti non è costante ma è influenzato da diversi fattori come il livello di vigilanza, attenzione, aspettativa e / o stress, (22) e possono tradursi sia in una facilitazione che in un effetto inibitorio sulla trasmissione nocicettiva.
Il corpo umano disponedi un potente sistema di controllo del dolore endogeno. I percorsi inibitori endogeni sono, ad esempio, attivati durante l’esercizio: la diminuzione della percezione del dolore dopo l’esercizio è osservato e dimostrato in soggetti in buona salute.
Questo effetto ipoalgesico dell’esercizio, spesso chiamato “analgesia esercizio indotta”, è spiegato dal rilascio di oppioidi endogeni, fattori di crescita e altri potenti meccanismi inibitori (“Inibizione discendente”) orchestrato dal nervoso sistema centrale e dal cervello (21).
Nello stesso tempo una prolungata o intensa attività può aumentare la responsività neuronale e causare sensibilizzazione (13).
La sensibilizzazione, definita come una maggiore risposta agli stimoli, può presentarsi sia nei tessuti periferici che nel sistema nervoso centrale compreso il cervello.
Quando il dolore persiste, si verifica un adattamento dei nocicettori unimodali risultando in una maggiore reattività dovuta a rilascio di mediatori da vari sistemi (25).
Questo processo è noto come iperalgesia primaria o sensibilizzazione periferica e serve come azione protettiva per evitare ulteriori danni ai tessuti lesi (15).
Iperalgesia secondaria si riferisce invece alla maggiore reattività dei neuroni della dorsale del corno.(15).
Comunque è opportuno sottolineare che l’iperalgesia non è indice di una condizione cronica infatti anche nel dolore acuto si possono realizzare condizioni di iperalgesia.
L’attività del proencefalo inteso come elaborazioni storiche ed emozioni, è in grado di modulare l’esperienza del dolore clinico e può contribuire al meccanismo di sensibilizzazione centrale (26). Visto il suo effetto di facilitazione sulla trasmissione nocicettiva, questo è spesso chiamato “sensibilizzazione emotiva cognitiva ” (27).
Un passo importante nella valutazione del dolore dunque è la valutazione del meccanismo del dolore predominante che andrà a condizionare l’approccio terapeutico, molto diverso a seconda del meccanismo del dolore sottostante (28).
La classificazione, dunque, che è sempre più utilizzata nei pazienti con dolore muscolo scheletrico è la differenziazione tra nocicettivo, neuropatico e alterazione del dolore centrale (28,29).
Il dolore nocicettivo si riferisce al dolore che origina dal reale o minacciato danno ai tessuti con attivazione di nocicettori.
Il dolore neuropatico è definito come dolore causato da una lesione o da una malattia che colpisce il sistema nervoso somatosensoriale (5).
Dunque, importante nella pratica clinica, useremo il termine nocicettivo per descrivere il dolore trasmesso dal sistema nervoso somatosensoriale normalmente funzionante, mentre definiremo dolore neuropatico quando potremo dimostrare un’anomala funzione dello stesso (30).
La terza categoria, il dolore psichico, colpisce pazienti con elaborazione alterata del dolore centrale
(dolore nociplastico). L’associazione internazionale per lo studio di il dolore definisce quest’ultimo come dolore derivante da nocicezione alterata con nessuna chiara evidenza di dani ai tessuti che causano l’attivazione di nocicettori periferici o evidenza di una malattia o lesione del sistema somatosensoriale (5).
Per aggiungere complessità alla complessità, numerose sono le osservazioni di pazienti con modelli di dolore misto.41 Ad esempio,un paziente con lombalgia che irradia alla gamba può soffrire di una combinazione di dolore alla schiena nocicettivo (originario da una struttura muscolo-scheletrica come disco, muscolo, legamento o articolazione) e dolore neuropatico alla gamba, causato dall’irritazione del nervo (radicolopatia). Anche una combinazione di dolore centrale alterato con dolore nocicettivo o neuropatico è stato riportato nei pazienti (31).
Il più delle volte il dolore nei pazienti emofilici è di natura nocicettivo, tuttavia alcuni ricercatori hanno osservato che una percentuale non indifferente di questi pazienti presenta spesso anche un dolore neuropatico dominante (32,33) con segni anche di meccanismi di dolore centrale alterato.
APPROCCIO TERAPEUTICO
Nella pratica clinica osserviamo che la maggior parte dei pazienti emofilici è colpito da dolore acuto nel corso dei sanguinamenti e soffre di dolore cronico dovuto a sinovite o artropatia.
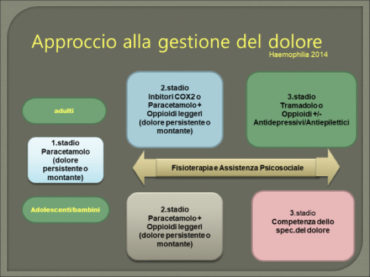
In linea generale attualmente le strategie del dolore per i pazienti emofilici suggeriscono un approccio graduale secondo una scala del dolore tenendo conto dei rischi specifici di questi pazienti. Ovviamente nel dolore acuto (emartro) la terapia sostitutiva è il primo passo. A seguire nel dolore persistente si consiglia terapia antalgica con paracetamolo, e negli adulti possiamo utilizzare anche i COX2. Anche i FANS possono avere un ruolo utile avendo ben presente il rischio gastrolesivo. Il terzo passaggio consiste nell’utilizzo degli oppioidi.
Il trattamento farmacologico del dolore neuropatico o i meccanismi di dolore centrale alterati sono diversi da quelli del dolore nocicettivo e dovrebbero includere ad esempio antidepressivi triciclici e inibitori della ricaptazione della serotonina-norepinefrina (34,35,36).
Sebbene il meccanismo di inibizione discendente del dolore è principalmente biologico, esso è influenzato da cognizioni inappropriate, emozioni, ipervigilanza e comportamenti somatizzanti. Queste condizioni di fatto inibiscono il controllo endogeno del dolore e di contro promuovono la sensibilizzazione centrale (37).
La consapevolezza dello stimolo nocivo, la sua elaborazione cognitiva, l’influenza dell’ambiente (es. valori culturali e sociali) , l’apprendimento da esperienze precedenti portano i soggetti ad agire sul loro dolore, cioè a determinare il loro comportamento doloroso. Sembra quindi che approcci pscicoterapici e psicosociali possono essere di estrema utilità nella gestione del dolore (38).
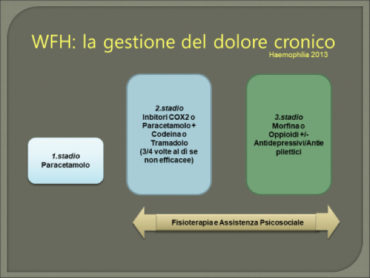
Lo sviluppo della sensibilizzazione centrale sembra inoltre essere dipendente dal tempo (stimolazione nociva > 3 mesi) mentre la fisioterapia precoce (ad esempio il trattamento miofasciale e l’allenamento per il controllo motorio effettuato comunque con cautela per evitare la stimolazione nociva da procedura) sembra possa prevenire la cronicità (36). Alcuni studi hanno dimostrato come tempi di precoce intervento della fisioterapia abbiano , con un esercizio moderato , un discreto effetto ipoalgesico associato ad un aumento della soglia del dolore(34).
CONCLUSIONE
Capire la complessità del dolore, dunque, è l’unico percorso che potrà permette di valutare e gestire al meglio il dolore (39,40).
La ricerca futura dovrà aiutare il clinico ad individuare i pazienti che soffrono di dolore prevalentemente neuropatico da quelli che hanno un’elaborazione del dolore alterato a livello centrale o da quelli che presenteranno un dolore di tipo misto.
Studi futuri dovranno anche valutare l’effetto dei farmaci antidolorifici sulla valutazione del dolore, come è già stato fatto nei pazienti con dolore cronico in altre condizioni cliniche.
Infine emerge sempre più l’importanza di un’approccio biopsicosociale al dolore, la comprensione dell’influenza delle componenti psicologiche e culturali nella percezione del dolore.
RIFERIMENTI
1. Witkop M, Neff A, Buckner TW, et al. Self-reported prevalence,description and management of pain in adults with haemophilia: methods, demographics and results from the Pain, Functional Impairment, and Quality of life (P-FiQ) study. Haemophilia. 2017;23:556‐565.
2. Forsyth AL, Witkop M, Lambing A, et al. Associations of quality of life, pain, and self-reported arthritis with age, employment, bleed rate, and utilization of hemophilia treatment center and health care provider services: results in adults with hemophilia in the HERO study. Patient Prefer Adherence. 2015;9:1549‐1560.
3. Wallny T, Hess L, Seuser A, Zander D, Brackmann HH, Kraft CN. Pain status of patients with severe haemophilic arthropathy. Haemophilia. 2001;7:453‐458.
4. Timmer MA, Pisters MF, de Kleijn P, de Bie RA, Fischer K, Schutgens RE. Differentiating between signs of intra-articular joint bleeding and chronic arthropathy in haemophilia: a narrative review of the literature. Haemophilia. 2015;21:289‐296.
5. Merskey H, Bogduk N. Classification of Chronic Pain. IASP Task Force on Taxonomy, 2nd edn. Seattle, WA: IASP Press; 1994.
6. National Pharmaceutical Council and Joint Commission on Accreditation of Healthcare Organizations. Pain: Current Understanding of Assessment, Management, and Treatments. Reston, VA: National Pharmaceutical Council, Incorporated; 2001.
7. Witkop M, Lambing A, Kachalsky E, Divine G, Rushlow D, Dinnen J. Assessment of acute and persistent pain management in patients with haemophilia. Haemophilia. 2011;17:612‐619.
8. Ceponis A, Wong-Sefidan I, Glass CS, von Drygalski A. Rapid musculoskeletal ultrasound for painful episodes in adult haemophilia patients. Haemophilia. 2013;19:790‐798.
9. Humphries TJ, Kessler CM. The challenge of pain evaluation in haemophilia: can pain evaluation and quantification be improved by using pain instruments from other clinical situations? Haemophilia. 2013;19:181‐187.
10. Holstein K, Klamroth R, Richards M, et al. Pain management in patients with haemophilia: a European survey. Haemophilia. 2012;18:743‐752.
11. Wallny T, Lahaye L, Brackmann HH, Hess L, Seuser A, Kraft CN. Clinical and radiographic scores in haemophilic arthropathies: how well do these correlate to subjective pain status and daily activities? Haemophilia. 2002;8:802‐808.
12. Lee YC, Nassikas NJ, Clauw DJ. The role of the central nervous system in the generation and maintenance of chronic pain in rheumatoid arthritis, osteoarthritis and fibromyalgia. Arthritis Res Ther. 2011;13:211.
13. Woolf CJ. Central sensitization: implications for the diagnosis and treatment of pain. Pain. 2011;152(3 Suppl):S2‐S15.
14. Marchand S. The physiology of pain mechanisms: from the periphery to the brain. Rheum Dis Clin North Am. 2008;34:285‐309.
15. Roussel NA, Nijs J, Meeus M, Mylius V, Fayt C, Oostendorp R. Central sensitization and altered central pain processing in chronic low back pain: fact or myth? Clin J Pain. 2013;29:625‐638.
16. Lluch E, Torres R, Nijs J, Van Oosterwijck J. Evidence for central sensitization in patients with osteoarthritis pain: a systematic literature review. Eur J Pain. 2014;18:1367‐1375.
17. Brooks J, Tracey I. From nociception to pain perception: imaging the spinal and supraspinal pathways. J Anat. 2005;207:19‐33.
18. Zhuo M. Cortical excitation and chronic pain. Trends Neurosci. 2008;31:199‐207.
19. Melzack R. From the gate to the neuromatrix. Pain. 1999;Supp 6:S121‐S126.
20. Staud R. Abnormal endogenous pain modulation is a shared characteristic of many chronic pain conditions. Expert Rev Neurother. 2012;12:577‐585.
21. Millan MJ. Descending control of pain. Prog Neurobiol. 2002;66:355‐474.
22. Rygh LJ, Tjølsen A, Hole K, Svendsen F. Cellular memory in spinal nociceptive circuitry. Scand J Psychol. 2002;43:153‐159.
23. Nijs J, Meeus M, Van Oosterwijck J, et al. Treatment of central sensitization in patients with ‘unexplained’ chronic pain: what options do we have? Expert Opin Pharmacother. 2011a;12:1087‐1098.
24. Kaya S, Hermans L, Willems T, Roussel N, Meeus M. Central sensitization in urogynecological chronic pelvic pain: a systematic literature review. Pain Physician. 2013;16:291‐308.
25. Purves D, Augustine GJ, Fitzpatricet D, et al. Neuroscience. Sunderland: Sinauer Associations Inc.; 1997.
26. Zusman M. Forebrain-mediated sensitization of central pain pathways: ‘non-specific’ pain and a new image for MT. Man Ther. 2002;7:80‐88.
27. Brosschot JF. Cognitive-emotional sensitization and somatic health complaints. Scand J Psychol. 2002;43:113‐121.
28. Nijs J, Torres-Cueco R, van Wilgen CP, et al. Applying modern pain neuroscience in clinical practice: criteria for the classification of central sensitization pain. Pain Physician. 2014;17:447‐457.
29. Smart KM, Blake C, Staines A, Doody C. The Discriminative validity of “nociceptive”, “peripheral neuropathic”, and “central sensitization” as mechanisms-based classifications of musculoskeletal pain.Clin J Pain. 2011;27:655‐663.
30. La Cesa S, Tamburin S, Tugnoli V, et al. How to diagnose neuropathic pain? The contribution from clinical examination, pain questionnaires and diagnostic tests. Neurol Sci. 2015;36:2169‐2175.
31. Nijs J, Apeldoorn A, Hallegraeff H, et al. Low back pain: guidelines for the clinical classification of predominant neuropathic, nociceptive, or central sensitization pain. Pain Physician. 2015;18:E333‐E346.
32. Krüger S, Hilberg T. Neuropathic pain in patients with haemophilia, that is the question. Hamostaseologie. 2015;35(Suppl 1):S5‐S9.
33. Krüger S, Weitz C, Runkel B, Hilberg T. Pain sensitivity in patients with haemophilia following moderate aerobic exercise intervention. Haemophilia. 2016;22:886‐893.
34. van Vulpen LFD, Schutgens REG, Coeleveld K, et al. IL-1beta, in contrast to TNFalpha, is pivotal in blood-induced cartilage damage and as such a potential target for therapy. Blood. 2015;126:2239‐2246.
35. Van Meegeren ME, Van Veghel K, De Kleijn P, et al. Joint distraction results in clinical and structural improvement of haemophilic ankle arthropathy: a series of three cases. Haemophilia. 2012;18:810‐817
36. Acharya SS, Schloss R, Dyke JP, et al. Power Doppler sonography in the diagnosis of hemophilic synovitis–a promising tool. J Thromb Haemost. 2008;6:2055‐2061.
37. Nijs J, Van Houdenhove B. From acute musculoskeletal pain to chronic widespread pain and fibromyalgia: application of pain neurophysiology in manual therapy practice. Man Ther. 2009;14:3‐12.
38. Linton SJ, Shaw WS. Impact of psychological factors in the experience of pain. Phys Ther. 2011;91:700‐711.
39. LFD van Vulpen, K. Holstein, C. Martinoli Joint disease in haemophilia: Pathophysiology, pain and imaging Haemophilia. 2018;24(Suppl. 6):44–49.
40. NA Roussel Gaining insight into the complexity of pain in patients with haemophilia: State-of-the-art review on pain processing, Haemophilia. 2018;24(Suppl. 6):3–8
*Le tabelle sono state redatte a cura dell’estensore dell’articolo



